洛拉替尼片(博瑞纳)中文说明书[通用名称] 洛拉替尼片[商品名称] 博瑞纳® / LORBRENA®[英文名称] Lorlatinib Tablets...
2026-04-21 304 洛拉替尼片 博瑞纳 药品说明书 ALK阳性NSCLC 肺癌靶向药

【通用名称】赛沃替尼片
【商品名称】沃瑞沙®/ORPATHYS®

【英文名称】Savolitinib Tablets
【汉语拼音】Saiwotini Pian
【成份】本品主要成分为赛沃替尼。
化学名称:1-[(1S)-1-(咪唑并[1,2-a]吡啶-6-基)乙基]-6-(1-甲基-1H-吡唑-4-基)-1H-[1,2,3]三唑并[4,5-b]吡嗪
化学结构式:
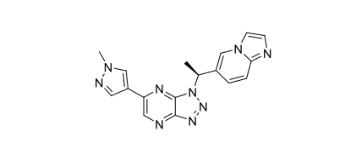
分子式:C17H15N9
分子量:345.36
【性状】薄膜衣片,除去包衣后显白色至黄色。
【适应症】本品用于含铂化疗后疾病进展或不耐受标准含铂化疗的、具有间质-上皮转化因子(MET)外显子14跳变的局部晚期或转移性非小细胞肺癌成人患者。
本适应症是基于一项单臂临床试验的客观缓解率和缓解持续时间结果给予的附条件批准。本适应症的完全批准将取决于后续开展的确证性试验的临床获益。
【规格】(1)100 mg;(2)200 mg。
【用法用量】本品需在有肿瘤治疗经验的医生指导下使用。使用本品治疗前必须明确有经充分验证的检测方法检测到 MET 外显子 14 跳变阳性。
推荐剂量和服用方法
对于体重≥50 公斤的患者,建议起始剂量为 600 mg,每日一次口服,直到疾病进展或出现不可耐受的毒性。
对于体重<50 公斤的患者,建议起始剂量为 400 mg,每日一次口服,直到疾病进展或出现不可耐受的毒性。
建议每日相同时段在餐后即刻服用本品。
剂量调整
医生应在患者用药过程中密切监测,根据患者个体的安全性和耐受性调整用药,包括暂停本品、降低剂量或永久停用本品。
本品的剂量调整建议参见表 1,不良反应导致治疗调整的建议参见表 2。
表 1 赛沃替尼剂量调整建议
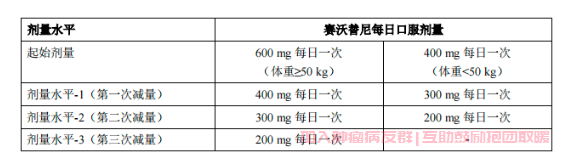
表 2 赛沃替尼不良反应导致治疗调整的建议

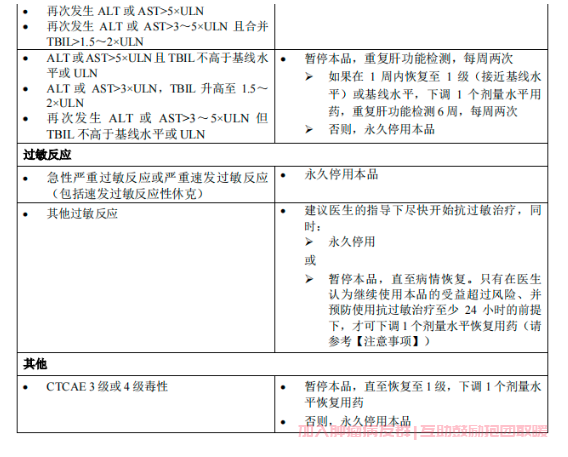
缩略语:ALT = 丙氨酸氨基转移酶;AST = 天门冬氨酸氨基转移酶;CTCAE = 常见不良反应事件评价标准;INR = 国际标准化比率;TBIL = 总胆红素;ULN = 正常值上限。
备注:不良反应的严重程度采用美国国立癌症研究所(NCI)常见不良事件评价标准(CTCAE)4.03 版进行分级。
特殊患者人群
肝功能不全:轻度肝功能不全的患者(总胆红素<ULN 和 ALT 或 AST>ULN;或 1.5×ULN>总胆红素>ULN 以及任意水平 ALT 或 AST)服用本品无需调整起始剂量。目前尚无中度和重度肝功能不全患者(总胆红素>1.5×ULN 以及任意水平 ALT 或 AST)的研究数据,因此中重度肝功能不全患者应在医生指导下慎用本品,并严密监测其肝功能(参见【药代动力学】)。
肾功能不全:轻度和中度肾功能不全患者服用本品无需调整起始剂量。目前尚无重度肾功能不全患者的研究数据,重度肾功能不全患者应在医生指导下谨慎服用本品,并严密监测其肾功能(参见【药代动力学】)。
儿童患者:尚无本品用于 18 岁以下儿童或青少年患者的临床数据。
老年患者:年龄≥65 岁患者无需调整起始剂量。
【不良反应】本说明书描述了在临床研究中观察到的判断为可能由本品引起的不良反应及其近似的发生率。由于临床研究是在各种不同条件下进行的,在一个临床研究中观察到的不良反应的发生率不能与另一个临床研究观察到的不良反应发生率直接比较,也可能不能反映临床实践中的实际发生率。
赛沃替尼的安全性数据来自于 5 项临床试验,总计有 345 例肿瘤患者接受本品单药治疗,其中有 338 例患者[含关键性 II 期研究的 70 例 MET 外显子 14 跳变的非小细胞肺癌患者(肺肉瘤样癌和其他非小细胞肺癌)]暴露于推荐剂量及以上(≥400 mg,每日一次)剂量水平。在接受≥400 mg 剂量的患者中,20.4%的患者因不良反应而暂停治疗;导致暂停治疗的不良反应(≥1%)为水肿(4.7%)、恶心(3.6%)、呕吐(3.6%)、发热(3.8%)、天门冬氨酸氨基转移酶升高(2.4%)、丙氨酸氨基转移酶升高(2.1%)、疲乏/乏力(1.8%)、食欲减退(1.5%)、贫血(1.5%)、皮疹(1.5%),以及肝功能异常(1.2%)。15.4%的患者因不良反应而减量;导致减量的不良反应(≥1%)为水肿(4.4%)、丙氨酸氨基转移酶升高(3.6%)、天门冬氨酸氨基转移酶升高(3.3%)、恶心(1.5%)、疲乏/乏力(1.2%)、发热(1.2%),以及肝功能异常(1.2%)。11.8%的患者(40 例)因不良反应而永久停药;导致永久停药的不良反应(≥1%)为肝功能异常(3.8%)、呕吐(1.5%)、丙氨酸氨基转移酶升高(2.1%),疲乏/乏力(1.2%)、水肿(1.2%)、天门冬氨酸氨基转移酶升高(1.2%),以及严重过敏反应(1.2%)。
在接受≥400 mg 剂量的患者中,常见(≥10%)不良反应为恶心(44.7%)、水肿(40.5%)、疲乏/乏力(31.1%)、呕吐(31.1%)、食欲减退(21.0%)、低白蛋白血症(17.2%)、贫血(16.6%)、发热(15.7%)、腹泻(13.6%),以及肝功能异常(11.8%)。
常见(≥10%)实验室检查异常包括天门冬氨酸氨基转移酶升高(18.0%)和丙氨酸氨基转移酶升高(16.3%)。
在接受≥400 mg 剂量的患者中发生的不良反应详见表 3。
表3.在接受推荐剂量及以上(≥400 mg,每日一次)赛沃替尼的患者中不良反应的发生情况
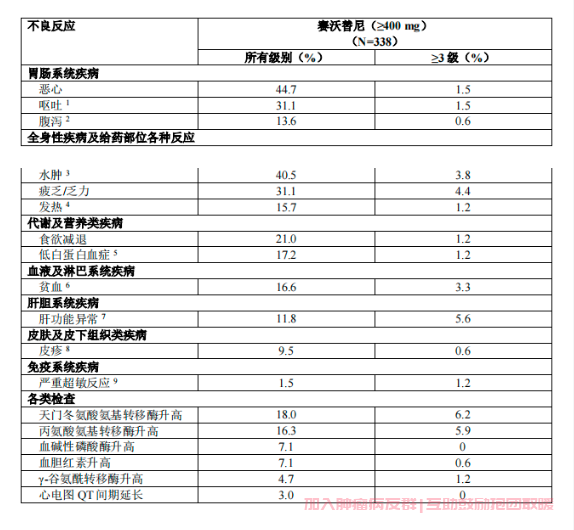
本说明书在确定不良反应的发生率时采用的是报告的所有不良事件(无论相关性)的发生率。
1. 呕吐包括呕吐、干呕;
2. 腹泻包括腹泻、排便频率增加;
3. 水肿包括外周水肿、水肿、面部水肿、外周肿胀、肿胀、局部水肿、眼睑水肿、全身性水肿、阴囊水肿、睾丸水肿、牙龈肿胀、眼水肿、生殖器水肿、阴茎水肿;
4. 发热包括发热、流感样症状、寒战、体温升高、高热;
5. 低白蛋白血症包括血白蛋白降低、低白蛋白血症;
6. 贫血包括贫血、血红蛋白降低、红细胞计数下降;
7. 肝功能异常包括肝功能异常、药物诱导的肝损伤、肝损伤、肝病损、肝性脑病、肝脏毒性、肝脏疾病;
8. 皮疹包括皮疹、斑丘疹、药疹、丘疹、红斑性发疹、瘙痒性皮疹、水泡疹、痤疮样皮炎、过敏性皮炎、皮炎、多形性红斑、中毒性皮疹;
9. 严重超敏反应包括药物性超敏反应、速发过敏反应性休克、超敏反应。
特定的不良反应
肝毒性:在接受≥400 mg 剂量的患者中,肝毒性主要表现为天门冬氨酸氨基转移酶升高、丙氨酸氨基转移酶升高、低白蛋白血症、肝功能异常、血胆红素升高、碱性磷酸酶升高等肝功能检查异常,大多数为 1~2 级;发生率>1.5%的≥3 级的肝毒性事件包括天门冬氨酸氨基转移酶升高(6.2%)、丙氨酸氨基转移酶升高(5.9%)、肝功能异常(5.6%)。从开始服药到不良反应发生的中位时间为 31 天。另外,在肝毒性事件中,药物诱导的肝损伤(DILI)(所有级别)的发生率为 1.2%,≥3 级的 DILI 的发生率为 0.9%。在所有肝毒性事件中,有 1 例(0.3%)致死性病例。
发热:在接受≥400 mg 剂量的患者中,发热相关事件主要表现为发热、寒战、高热和流感样症状等,从开始服药到不良反应发生的中位时间为 20 天,大部分为 1~2 级,没有死亡的病例报告。
严重过敏反应:在接受≥400 mg 剂量的患者中,符合严重不良事件标准的过敏反应包括药物性超敏反应(0.9%)、速发过敏反应性休克(0.3%)、超敏反应(0.3%),从开始服药到不良反应发生的中位时间为 15 天,没有死亡病例报告。
水肿:在接受≥400 mg 剂量的患者中,水肿相关事件包括外周水肿、水肿、面部水肿、外周肿胀、肿胀等,从开始服药到不良反应发生的中位时间为 50 天,大多数为 1~2 级;发生率>1.5%的 3 级水肿事件仅包括外周水肿(2.4%),没有死亡病例报告。
【禁忌】有本品严重过敏史者或对本品任何成分过敏者禁用。
妊娠、哺乳期妇女禁用。
【注意事项】肝毒性:临床研究中观察到本品可能引起肝功能检查异常和药物诱导的肝损伤等,多为 1~2级,有 1 例(0.3%)致死性病例。详情可参见“特定不良反应”。
临床研究中从开始接受本品至发生肝毒性的中位时间为 31 天(范围 1~420 天),经过保肝治疗以及剂量调整或暂停用药后,通常可恢复至≤1 级或用药前水平。
使用本品前存在肝脏功能异常风险因素(如肝胆疾病、肝转移、肝功能异常等)的患者需要全面谨慎地评估。治疗期间应定期监测肝功能(如转氨酶及血胆红素),建议开始用药后前 3 个月内每周监测。3 个月后可根据肝功能检查的结果调整监测频率,如每2-3 周评估肝功能,必要时调整剂量或停用本品。(参见【用法用量】中的“剂量调整”)
严重过敏反应:临床研究中,从开始接受本品至发生严重过敏反应的中位时间为 15 天(范围 10~90天)。
临床研究中观察到本品可引起发热、寒战和流感样症状,从开始接受本品至发热的中位时间为 20 天(范围 1~620 天)。
本品引起超敏反应(表现为一系列症状,包括但不限于:药物相关性发热、皮肤过敏反应、肝酶升高、血细胞下降、肌痛/关节痛)。这些反应可在用药后数天至数周内发生,但大多发生在用药后六周内。
临床研究中观察到某些开始表现为超敏反应的患者短期停药后,当恢复本品治疗时会出现急性严重超敏反应,包括速发过敏反应。
患者疑似发生本品相关超敏反应(排除已确认的感染病因)时,应根据患者具体病情给予相应的治疗(如抗组胺药、糖皮质激素、退热药等)并停用本品。待症状恢复后,只有在医生认为继续使用本品的受益超过风险时方可减量用药。在恢复本品前至少 24 小时开始预防和伴随应用抗过敏药物(如糖皮质激素和抗组胺药),恢复本品用药当天必须在院内留观 24 小时,恢复本品用药后需继续使用抗过敏药物至少 1 周,并由医生判断是否仍需继续使用抗过敏药物。一旦发生急性超敏反应或速发过敏反应,必须立即进行医学干预,并应永久停用本品,参见【用法用量】。
【孕妇及哺乳期妇女用药】避孕:必须告知育龄女性本品可能伤害胎儿。育龄女性服用本品前需做妊娠检查以排除妊娠。
育龄女性需在治疗期间和治疗后 1 个月内确保有效避孕。
男性患者需在治疗期间和治疗后 6 个月内确保有效避孕。
妊娠:动物研究显示本品具有胚胎和胎儿毒性,尚无本品对孕妇影响的临床研究。
不建议在妊娠期间使用本品。
哺乳:尚不了解本品及其代谢物是否可经人乳分泌。由于对胎儿的潜在风险,应建议母亲在接受本品治疗过程中避免母乳喂养。
生育力:尚无关于本品影响生育力的临床数据,因此本品对男性和女性生育力的影响不详。更多信息请参见【药理毒理】。
【儿童用药】尚无本品用于 18 岁以下儿童或青少年患者的临床资料,故本品用于 18 岁以下儿童和青少年的安全性和有效性尚不明确。
【老年用药】在本品当前进行或已完成的临床研究中,共 156 例老年患者(≥65 岁)接受了本品治疗,占暴露总人群的 45.2%。与<65 岁患者比较,老年患者的用药的安全性特征无明显差异。
【药物相互作用】临床前体外研究显示,赛沃替尼可通过多种代谢酶代谢,主要包括 CYP1A2、CYP3A4 和 CYP3A5 等。临床药代动力学研究中,与伊曲康唑 200 mg 每日一次(一种强效 CYP3A4 抑制剂)合并用药不会对本品的暴露量产生临床显著性影响(血浆药物浓度-时间曲线下面积(AUC)和峰浓度(Cmax)增加均小于 15%),因此,CYP3A4 抑制剂不太可能对本品的暴露量产生显著影响。在另一项临床药代动力学研究中,合并服用利福平(一种强效 CYP3A4 诱导剂)600 mg 每日一次连续 8 天,会使本品的 AUC 和 Cmax分别降低 61%和 55%,建议应避免本品和 CYP3A4 的强诱导剂(如苯妥英、利福平和卡马西平)同时使用。CYP3A4 的中度诱导剂(如波生坦、依法韦仑、依曲韦林和莫达非尼)对本品暴露量的影响情况未知,但同样可能降低本品的暴露量,因此本品也应谨慎或尽可能避免与 CYP3A4 中度诱导剂合用。对于贯叶连翘(St. John’s Wort)及其提取物应在本品服用前 3 周禁服。目前尚无临床试验证实 CYP1A2 强效抑制剂对本品的影响,因此根据体外试验结果,本品首次服用前 1 周内及后续服用本品期间,患者应避免使用强效CYP1A2 抑制剂。
在体外,赛沃替尼对 CYP2C8 和 CYP2C9 具有中等程度的可逆抑制,对 CYP2D6 和CYP3A4/5 有弱的可逆抑制。赛沃替尼代谢产物 M2 和 M3 对 CYP2C8、CYP2C9 和CYP3A4 均有抑制作用,M2 对 CYP1A2 和 CYP2D6 也存在抑制作用。临床药代动力学研究中,本品 600 mg 单次给药与咪达唑仑(一种敏感的 CYP3A4/5 底物)合用,咪达唑仑暴露量无明显变化(Cmax 降低 16%,AUC 降低小于 5%),因此本品可以与为 CYP3A4/5底物的药物合用。尚无法排除对 CYP2C8、CYP2C9 和 CYP2D6 敏感或治疗窗窄的底物的影响,因此应谨慎服用敏感或治疗窗窄的 CYP2C8、CYP2C9 和 CYP2D6 底物的药物,并监测其与赛沃替尼合用可能导致这些药物暴露量的增加所带来的安全性风险。
赛沃替尼和 M2对有机阳离子转运体(OCT)2、多药及毒素外排转运蛋白(MATE)1和 MATE2K有一定的抑制作用,因此应慎用二甲双胍,并监测由于二甲双胍暴露量增加可能带来的风险。
赛沃替尼对 P-糖蛋白(P-gp)有弱的抑制作用,因此应慎用敏感的 P-gp 底物并监测可能导致的 P-gp 底物暴露量的增加所带来的安全性风险。
赛沃替尼不太可能与 CYP1A2、CYP2A6、CYP2B6、CYP2C19、CYP2E1、II 相代谢酶如葡萄糖醛酸转移酶(UGT)1A1 和 UGT2B7、乳腺癌耐蛋白(BCRP)、有机阴离子转运多肽(OATP)1B1 和 1B3、有机阴离子转运体 1 和 3(OAT1 和 OAT3)等的底物发生药物相互作用。
在临床药代动力学研究中,合并给予法莫替丁(40 mg 单次给药)并不会对本品的暴露量产生临床相关性影响(Cmax降低 21%,AUC 降低小于 15%)。本品可与改变胃内 pH值的药物合并使用,无需任何限制。
在健康受试者中进行的全面 QT 研究显示,单次口服赛沃替尼 600 mg,可能引起相关的 QTc延长,且与赛沃替尼浓度存在正相的线性关系。因此应谨慎合用其他可能导致 QTc延长的药物,并密切观察可能的安全性风险。
【药物过量】目前尚不清楚过量服用本品可能产生的危害。
本品用药过量没有特定的解毒药。如疑似药物过量,应立即停用本品,对患者进行密切观察,必要时采取最佳支持治疗。
【临床试验】MET 外显子 14 跳变的非小细胞肺癌
研究 2016-504-00CH1 是一项在 MET 外显子 14 跳变的局部晚期或转移性非小细胞肺癌患者中进行的多中心、单臂、开放的 II期研究,评价赛沃替尼单药治疗的疗效、安全性和耐受性。
入组患者为既往接受含铂化疗失败[疾病进展或毒性不耐受]或经医生评估不适合进行标准治疗、MET 外显子 14 跳变且 EGFR、ALK、ROS1 敏感基因变异阴性、经组织学诊断的局部晚期或转移性非小细胞肺癌(含肺肉瘤样癌和其他非小细胞肺癌)患者。
共 70 例 MET 外显子 14 跳变的非小细胞肺癌患者接受赛沃替尼 600 mg 或 400 mg(依据基线体重)每日一次口服,直至疾病进展或出现不能耐受的毒性。
肿瘤评估标准采用实体瘤疗效评价标准(RECIST)1.1 版,肿瘤评估的时间点为每 6周进行一次;治疗一年后每 12 周评估一次。
入组的 70 例患者全部被纳入全分析集。
入组患者的平均年龄(标准差)为 68.9(7.9)岁,其中大部分为高龄(≥65 岁的患者占 77.1%,≥75岁的患者占 22.9%);男性 41 例(58.6%);28例(40.0%)例患者为吸烟者;基线时美国东部肿瘤协作组(ECOG)体力状况评分为 0 分的患者有 12 例(17.1%),1 分的有 57 例(81.4%),3 分的有 1 例(1.4%);疾病分期为 IV 期的患者有 65 例(92.9%),其余 5 例(7.1%)均为 III 期;病理诊断为肺肉瘤样癌的患者有 25 例(35.7%),其他非小细胞肺癌的患者为 45 例(64.3%);42 例(60.0%)患者既往接受过针对晚期肿瘤的抗肿瘤系统药物治疗。
研究的主要疗效终点为独立阅片委员会(IRC)评估的客观缓解率,次要疗效终点包括疾病控制率、无进展生存期、缓解持续时间、起效时间、6 个月的无进展生存率和总生存期等。有效性的分析结果见表 4。
表 4.赛沃替尼的有效性结果(IRC 评估结果)–关键性 II 期临床研究
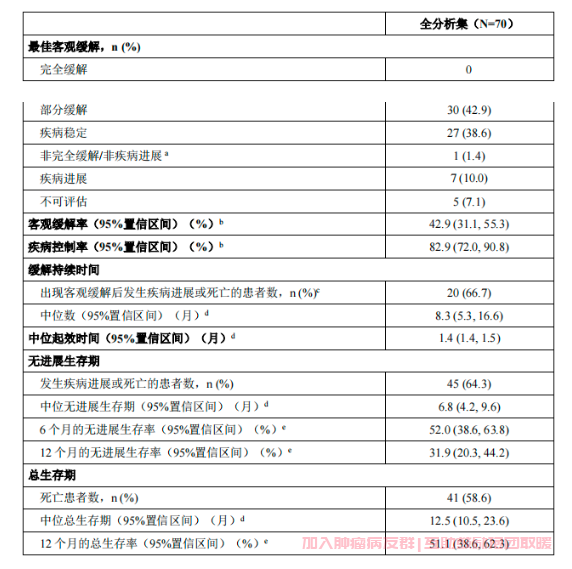
缩写:IRC = 独立阅片委员会。
数据截止日期:2020 年 08 月 03 日。
备注:根据方案规定,完全缓解或部分缓解均为经确认的完全缓解或部分缓解。
a. 一例患者经 IRC 评估基线无可测量病灶,故最佳疗效为非完全缓解/非部分缓解;
b. 客观缓解率或疾病控制率的精确 95%置信区间依据 Clopper-Pearson 方法计算;
c. 百分比基于 IRC 评估的获得客观缓解的患者数;
d. 采用 Kaplan-Meier 方法以及基于 Brookmeyer-Crowley 方法计算双侧 95%置信区间;
e. 采用 Kaplan-Meier 方法和 Green-World 公式计算,并进行双对数转换。
【药理毒理】药理作用
赛沃替尼可选择性抑制 MET(Mesenchymal-epithelial transition factor,细胞-间质表皮转化因子)激酶的活性,可抑制 MET 激酶的磷酸化,对 MET 基因扩增以及 MET 14 号外显子跳变的肿瘤细胞增殖有明显的抑制作用。在多种 MET 异常的人源肿瘤裸鼠移植模型中,赛沃替尼对肿瘤生长具有抑制作用。
毒理研究
遗传毒性:赛沃替尼 Ames 试验、中国仓鼠肺成纤维细胞染色体畸变试验和小鼠体内骨髓微核试验结果均为阴性。
生殖毒性:生育力和早期胚胎发育毒性试验中,雄性大鼠于交配前 4 周至交配后 2 周、雌性大鼠于交配前 2 周至妊娠第 7 天经口给予赛沃替尼 50、150、500 mg/kg/天(以体表面积计,分别相当于临床最大推荐剂量(MRHD)600mg/天的 0.7、2、6.7 倍),高剂量下可见雌雄动物体重明显减轻伴随摄食量明显下降,雄鼠睾丸相对重量明显升高,交配天数明显增加,授(怀)孕率明显降低以及活胎数量降低。亲代雌雄动物生育力和早期胚胎发育的未见不良反应剂量(NOAEL)均为 150mg/kg/天。
胚胎-胎仔发育毒性试验中,妊娠大鼠于妊娠第 6~16 天经口给予赛沃替尼 7.5、150 mg/kg/天(以 AUC 计,分别相当于 MRHD 的 0.5、9.3 倍),孕鼠体重和/或体重增长量降低,妊娠子宫重量、胎仔和活胎重量减轻,高剂量下晚期吸收胎和死胎数增加。胎仔可见剂量相关性的内脏(舌、脑、脐动脉)和/或骨骼(肩胛骨、股骨、中轴骨、盆骨)畸形和/或变异。妊娠兔于妊娠第 6~18 天经口给予赛沃替尼 1、15、150 mg/kg/天(以 AUC计,分别相当于 MRHD 的 0.2、4.6、45 倍),高剂量组母体可见与给药相关的体重、摄食量降低以及无粪便和尿液变色临床症状,中、高剂量组均可见胎仔外观和骨骼畸形和/或变异,兔胚胎-胎仔发育毒性的 NOAEL 为 1mg/kg/天。
致癌性:尚未进行赛沃替尼的致癌性研究。
其他毒性:赛沃替尼体外 3T3细胞中性红摄取光毒性试验结果为阳性。大鼠体内光毒性试验结果为阴性,高剂量 500 mg/kg/天剂量下的平均血浆药物浓度为 59.8 μg/mL,约为人 MRHD 剂量下稳态血浆峰浓度的 20 倍。
大鼠和犬重复给予赛沃替尼后的主要毒性反应涉及肝脏、肺脏、心脏、内分泌系统(肾上腺、甲状腺)、泌尿系统(肾脏、膀胱、输尿管)、免疫系统(胸腺、脾脏、骨髓)以及生殖系统(仅犬,睾丸和附睾)等。
【药代动力学】在澳大利亚肿瘤患者(约 90%高加索人,10%亚洲人)中单次口服赛沃替尼,在100~1000 mg 剂量范围内药物暴露量(Cmax和 AUC)基本随剂量的增加而等比例增加。单次口服 600 mg 赛沃替尼后在中国晚期实体肿瘤患者中的 Cmax 几何均数为 2000(20.7%,N=4) ng/mL,AUC0-∞几何均数为 14600(11.3%,N=4) h∙ng/mL。中国晚期胃癌(N=14)和非小细胞肺癌(N=4)患者连续 21 天给药 600 mg 赛沃替尼以后可迅速到达稳态,第 1天和第 21 天 Cmax几何均数分别为 2200(52.9%,N=18)和 2860(37.9%,N=17) ng/mL,AUC0-τ几何均数分别为 15500(56.1%,N=18)和 19700(36.2%,N=17) h∙ng/mL,无明显蓄积。
吸收:赛沃替尼在人体内口服吸收迅速,在中国肿瘤患者中餐后口服 600 mg 赛沃替尼剂量下中位达峰时间为 2 小时。600 mg 剂量下的绝对口服生物利用度为 68.8%。在男性健康志愿者中进行的食物影响试验表明,食物对赛沃替尼的吸收程度和速度都有一定影响,进食高脂高热量餐(食物总热量 800~1000 卡路里且脂肪占食物总热量 50%以上)后服用赛沃替尼会延迟赛沃替尼的口服吸收约 2 小时(空腹和餐后 Tmax中位值分别为 2 小时和 4 小时)并增加其在体内的暴露量(餐后 Cmax和 AUC0-∞分别增加 2.7%和 17.1%)。
分布:赛沃替尼具有中等的表观分布容积(Vz:139 L),在人血浆中的蛋白结合率为71.3%,全血血浆分配比为 0.977。
代谢和排泄:赛沃替尼具有中等的总清除率(CL:29.2 L/h),肾清除率为 1.20 L/h,消除半衰期(t1/2)为 3.52 小时。在健康男性志愿者单次口服[14C] 赛沃替尼溶液 300 mg 后,采样期间排泄物(尿液和粪便)的给药放射性回收率平均值为 94.1% (尿: 55.7%,粪:38. 4%)。其中大约 3.1%的给药剂量以赛沃替尼原形经尿液排泄,提示赛沃替尼口服吸收后主要经肝脏代谢并通过肾脏排泄。
特殊人群:尚未针对特殊人群如老年人、儿童、肝肾功能损伤人群进行药代动力学研究。
【贮藏】密封,常温保存。
【包装】聚酰胺/铝/聚氯乙烯冷冲压成型固体药用复合硬片和药用铝箔热合密封的铝铝泡罩板。
200 mg:7 片/板,3 板/盒;7 片/板,2 板/盒;
100 mg:7 片/板,3 板/盒。
【有效期】24 个月
【执行标准】YBH08662021
【批准文号】(1)100mg:国药准字 H20210026;(2)200mg:国药准字 H20210027。
【药品上市许可持有人】企业名称:和记黄埔医药(上海)有限公司
地址:中国(上海)自由贸易试验区蔡伦路 720 弄 4 号
邮政编码:201203
电话号码:021-20673000
传真号码:021-20673186
咨询热线:400-658-6360
【生产企业】企业名称:上海合全医药有限公司
生产地址:中国(上海)自由贸易试验区意威路 31 弄 4 号
邮政编码:200131
电话号码:400-658-6360
网址:https://www.chi-med.com/sc
相关文章
洛拉替尼片(博瑞纳)中文说明书[通用名称] 洛拉替尼片[商品名称] 博瑞纳® / LORBRENA®[英文名称] Lorlatinib Tablets...
2026-04-21 304 洛拉替尼片 博瑞纳 药品说明书 ALK阳性NSCLC 肺癌靶向药
2026年是肺癌靶向药发展的关键一年。得益于新版国家医保药品目录的调整,大量高价靶向药实现了“降价+进医保”的双重利好,极大地降低了患者的经济负担。医...
2026-04-20 424 肺癌靶向药汇总表 2026年肺癌靶向药 肺癌靶向药价格 肺癌靶向药医保报销情况 肺癌EGFR靶向药有哪些 ALK阳性肺癌靶向药价格 KRAS G12C靶向药最新价格 肺癌靶向药怎么选 国产肺癌靶向药推荐

一、卵巢癌靶向药价格汇总(2026.04更新版)以下为目前临床常用/在研卵巢癌靶向药的价格、医保、上市状态详细汇总,方便患者及家属按需参考:药物名称研...
2026-04-08 430 卵巢癌靶向药价格汇总 2026.04 卵巢癌靶向药医保报销情况 卵巢癌靶向药上市状态 PARP抑制剂价格 贝伐珠单抗价格 索米妥昔单抗价格 帕博利珠单抗价格 肿瘤患友群 微信号zhongliuw

对于胶质瘤患者和家属来说,治疗过程中最关心的问题之一,就是靶向药、新药的价格、是否上市、能否医保报销。毕竟胶质瘤的治疗周期长、费用高,提前了解药物的价...
2026-04-01 497 胶质瘤靶向药价格 胶质瘤新药 2026 胶质瘤医保报销药物 贝伐珠单抗价格 达拉非尼泰菲乐价格 曲美替尼迈吉宁价格 伯瑞替尼万比锐价格 胶质瘤电场治疗 TTF 价格 胶质瘤靶向药上市状态

确诊EGFR突变肺癌,对很多患者和家属而言,是不幸中的万幸,作为肺癌最常见的敏感突变,靶向治疗为无数病友打开了长期生存的大门,但这条靶向抗癌路,依旧布...
2026-03-23 394 EGFR 突变肺癌病友群 EGFR突变肺癌 EGFR突变肺癌病友群 肺癌靶向治疗 EGFR靶向药耐药 肺癌病友互助

加入肿瘤互助群
已有10万+患友进群交流经验↓
10万+真实病友交流经验,广告勿扰
打开微信,点击右上角"+"号,粘贴微信号,搜索即可!添加管理受邀进群讨论!
发表评论